Letzte Aktualisierung am 17.05.2026 / #VerdientProvisionen / Bilder von der Amazon Product Advertising API
Defintion und Eigenschaften
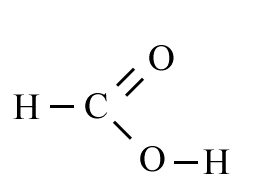
Ameisensäure ist der Trivialname der Methansäure. Sie ist die simpelste organische Säure und steht an erster Stelle der homologen Reihe der einfachen Carbonsäuren.
Hauptsächlich die für Carbonsäuren charakteristische Carboxy-Gruppe verleiht der Ameisensäure ihre Eigenschaften: Sie besitzt eine verhältnismäßig große Säurestärke sowie reduzierende Eigenschaften, welche durch das positiv polarisierte Kohlenstoffatom zu erklären sind.
Hinweis: Die beliebtesten Mittel gegen Ameisen listen wir u. a. auf der Unterseite Ameisen bekämpfen.
Beim Raumtemperatur und Standard-Luftdruck liegt Methansäure als eine farblose, leicht flüchtige Flüssigkeit mit sehr stechendem Geruch vor. Durch ihre sauren Eigenschaften kann es bei Kontakt mit der Haut oder den Schleimhäuten schnell zu Reizungen oder Verätzungen kommen.
Zudem können Hitze oder anderen Säuren dazu führen, dass sich die Ameisensäure selbst zersetzt, wobei das giftige Gas Kohlenstoffmonoxid sowie Wasser entstehen. Eine Aufbewahrung von höher konzentrierten Säurelösungen ist daher nur an einem kühlen und gut belüfteten Ort in einem Behälter mit der Möglichkeit zum Druckausgleich ratsam.
- VIELSEITIG EINSETZBAR – Ideal zum Entkalken von Maschinen, Beizen von Leder...
- STARKE KALKLÖSEKRAFT – Entfernt Kalk, Rost & Ablagerungen von Haushaltsgeräten...
- FÜR LEDER & KUNSTSTOFFE – Ideal zum Beizen, Imprägnieren & Farbfestigen von...
- HOCHWERTIGE QUALITÄT – Hochkonzentrierte Ameisensäure 73% für Reinigung...
- VIELSEITIG EINSETZBAR – Ideal zum Entkalken von Maschinen, Beizen von Leder...
- STARKE KALKLÖSEKRAFT – Entfernt Kalk, Rost & Ablagerungen von Haushaltsgeräten...
- FÜR LEDER & KUNSTSTOFFE – Ideal zum Beizen, Imprägnieren & Farbfestigen von...
- HOCHWERTIGE QUALITÄT – Hochkonzentrierte Ameisensäure 73% für Reinigung...
- VIELSEITIG EINSETZBAR – Ideal zum Entkalken von Maschinen, Beizen von Leder...
- STARKE KALKLÖSEKRAFT – Entfernt Kalk, Rost & Ablagerungen von Haushaltsgeräten...
- FÜR LEDER & KUNSTSTOFFE – Ideal zum Beizen, Imprägnieren & Farbfestigen von...
- HOCHWERTIGE QUALITÄT – Hochkonzentrierte Ameisensäure 73% für Reinigung...
Letzte Aktualisierung am 5.02.2026 / #VerdientProvisionen / Bilder von der Amazon Product Advertising API
Wo kommt Ameisensäure vor?
In der Natur kommt Ameisensäure häufig als Abwehrstoff in verschiedenen Tier und Pflanzenarten vor. Ameisen (Formicidae) aus der Unterfamilie der Schuppenameisen (Formicinae) beispielsweise besitzen spezialisierte Giftdrüsen gefüllt mit Ameisensäure zur Verteidigung. Wegameisen oder Waldameisen, die unter anderem in Mitteleuropa vorkommen, gehören in diese Unterfamilie und bedienen sich dieses Abwehrmechanismus.
Auch in manchen Quallenarten oder als Bestandteil der Abwehrstoffe in den Brennhaaren von Brennesseln kann Methansäure vorkommen. Der Große Ameisenbär hingegen zieht einen anderen Nutzen aus der Ameisensäure. Er selbst kann keine Magensäure produzieren und nutzt daher die Säure aus seiner hauptsächlichen Beute, Ameisen und Termiten, für seine Verdauung.
Auch im menschlichen Organismus kann Methansäure entstehen, wenn Methanol in den Stoffwechsel gelangt. Dieser wird erst zu Formaldehyd und dann zur Methansäure abgebaut, wodurch in höheren Konzentrationen der pH-Wert des Blutes absinkt (Azidose), was zu schwerwiegenden bis lebensbedrohlichen Komplikationen führen kann.
Wie wird die Methansäure gewonnen?

Während des 17. und 18. Jahrhunderts wurde Ameisensäure zunächst direkt aus Ameisen destilliert. Dazu wurden diese gesammelt, in der Regel ausgepresst und anschließend die Säure mit Hilfe einer Destillation abgeschieden. Im Jahr 1855 entwickelte Marcellin Berthelot eine weniger grausame Methode der Herstellung.
In einer zweistufigen Synthese und unter hohem Druck bei 210 °C wird zunächst aus Natriumhydroxid und Kohlenstoffmonoxid das Salz Natriumformiat gewonnen. Nach Zugabe von Schwefelsäure erhält man schließlich Ameisen- oder eben Methansäure sowie Natriumsulfat als weiteres Reaktionsprodukt. Aufgrund der Einfachheit dieses Verfahrens, wird es noch heute in industriellem Maßstab angewendet.
Ebenso fällt Ameisensäure als Nebenprodukt bei der Herstellung von Essigsäure durch die Oxidation von Acetaldehyd an und war in dieser Form bis in die 60er Jahre des 20. Jahrhunderts die primäre Form der Gewinnung.
Ameisensäure und moderne Einsatzgebiete
Hauptsächlich findet diese Säure in verschiedenen Industriezweigen Anwendung. Da sie biologisch in den allermeisten Ökosystemen gut abgebaut werden kann, ist ihre Verwendung in der Regel unkritisch. So wird sie beispielsweise zum Gerben von Tierhäuten bei der Lederherstellung eingesetzt, in der chemischen Industrie, um den pH-Wert zu regulieren, oder als Reaktionspartner bei chemischen Synthesen.
In der Imkerei hingegen ist Ameisensäure als Wirkstoff ein zugelassenes Mittel zur Bekämpfung der Varroamilbe, welche parasitär die Nachkommenschaft von Bienen befallen und schädigen kann.
Darüber hinaus besitzt die Methansäure weitere antimikrobielle Eigenschaften und wird daher in Desinfektionsmitteln verwendet, unter anderem bei der Einfuhr von Waren aus dem EU-Ausland zum Schutz gegen Tierseuchen.
Da die Salze der Ameisensäure wenig korrodierend wirken, werden sie teilweise als großflächiges Enteisungsmittel eingesetzt, zum Beispiel auf Landebahnen von Flughäfen. Als letztes Anwendungsgebiet sei die Reinigung von säurefesten Edelsteinen genannt, wobei die Methansäure genutzt wird, um Kalk oder andere Verunreinigungen aus dem Rohedelstein zu entfernen. Pharmazeutisch ist Ameisensäure auch in Mitteln zur Warzenbekämpfung enthalten.

Folgende Beiträge könnten Sie auch interessieren:
- Ameisen im Haus oder der Wohnung – Was ist zu tun?
Ameisen sind sehr nützliche Tiere, in den eigenen vier Wänden möchte man trotzdem nur ungern Insekten beherbergen. Lesen Sie unserer 15 Ratschläge gegen Ameisen im Haus. - Was hilft gegen Ameisen?
Fliegende Ameisen sind nicht etwa eine eigenständige Ameisenart, sondern nur zu bestimmten Jahreszeiten zu finden. Erfahren Sie mehr über die geflügelten Insekten und lernen Sie, wie man sie wieder los wird.
